Лечащий Врач #07, 2009
Головокружение, обусловленное патологией шейного отдела позвоночника
Головокружение и отоневрологические симптомы описаны при различных видах патологии в области шеи: травматических повреждениях шеи и спинного мозга [4, 5, 10], шейном остеохондрозе [2], окклюзии позвоночной артерии (ПА) [1, 3, 12] и инсультах, обусловленных повреждениями ПА [1, 11, 13, 15], диссекции ПА, в связи с движением шеи или манипуляцией на шейном отделе позвоночника [6, 7, 8, 9, 11, 14].
Выделение вертеброгенного головокружения обусловлено распространенностью патологии среди лиц молодого возраста, тяжестью течения заболевания, разнообразием симптоматики, возникновением инсультов при манипуляциях на шее.
Отличительной особенностью вертеброгенного головокружения является острое начало, связанное с определенной позицией головы (наклон вперед, запрокидывание назад, резкий поворот в сторону и др.), часто утром, после сна. Головокружение, которое возникает в результате изменения позиции головы, может быть обусловлено как раздражением внутреннего уха, так и центральных вестибулярных структур головного мозга (ствола, мозжечка). Компрессия артерий развивается при остеофитах и боковых грыжах дисков в унковертебральных областях, передних экзостозах суставных отростков, а также при подвывихе.
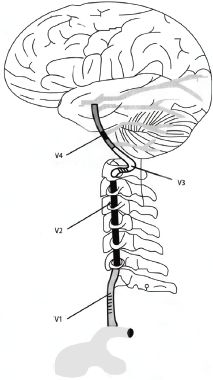 К анатомо-топографическим особенностям ПА относится расположение большей части ее экстракраниального отдела в канале позвоночника, где происходит ее смещение и сдавление остеофитами или суставными отростками при различных дегенеративных заболеваниях, в частности при остеохондрозе (рис. 1).
К анатомо-топографическим особенностям ПА относится расположение большей части ее экстракраниального отдела в канале позвоночника, где происходит ее смещение и сдавление остеофитами или суставными отростками при различных дегенеративных заболеваниях, в частности при остеохондрозе (рис. 1).
Отоневрологическое обследование пациента позволяет провести точную топическую диагностику, а также дифференциальную диагностику от периферического головокружения, обусловленного другими заболеваниями: болезнью Меньера, доброкачественным пароксизмальным позиционным головокружением, вестибулярным нейронитом.
Барре (1926), впервые обративший внимание на связь отоневрологических симптомов с патологией в области шеи, описал их под названием «задний шейный симпатический синдром», указывая при этом на значение связи головы и шеи при помощи симпатической нервной системы.
Показано, что углубленное исследование ПА с учетом не только диаметра и особенностей кровотока, но и с применением функциональных проб позволяет выявить моменты, важные для дифференциальной диагностики между гемодинамически значимой и незначимой экстравазальной компрессией ПА.
Повреждающее действие экстравазальных факторов компрессии направлено, прежде всего, на ее нервное сплетение. Раздражение позвоночного нерва, повышая тонус ПА, может уменьшить скорость объемного кровотока в ней на 30% от исходной величины, на 40% в ветвях основной артерии, в частности внутреннего уха [1].
Таким образом, функциональное состояние позвоночного нерва и структурные изменения ПА являются основой для развития недостаточности кровотока в вертебрально-базилярной системе (ВБС) на экстра- и интракраниальном уровне. Как подчеркивают различные авторы, кохлеовестибулярный синдром может развиваться при недостаточности кровообращения в ВБС как в области внутреннего уха, так и в области вестибулярных ядер и проводящих путей ствола головного мозга, мозжечка.
Кроме нарушений кровоснабжения ВБС, в патогенезе вертеброгенного головокружения также играет роль нарушенная проприоцептивная нервная импульсация со стороны структур шеи. Движения в измененных остеохондрозом и спондилоартрозом суставах шейных позвонков, дисках, а также возникающее тоническое напряжение мышц способствуют развитию неадекватной афферентной импульсации и неправильной оценке вестибулярной системой информации о позиции головы, что вызывает ощущение головокружения и нарушения равновесия.
Целью проведенной на базе НЦ неврологии РАМН работы было выявление клинических особенностей и отоневрологической симптоматики у больных с вертеброгенным головокружением на фоне патологических изменений в шейном отделе позвоночника, а также сопоставление вестибулярных нарушений со структурными изменениями ПА, уровнем артериального давления, состоянием внутренних яремных вен.
Нами проведено обследование 115 больных с острой и хронической недостаточностью кровообращения в ВБС, в том числе 47 пациентов с наличием дегенеративно-дистрофических изменений в шейном отделе позвоночника, из них у 33 — дегенеративные изменения (остеохондроз), у 9 — краниовертебральная патология, аномалия Киммерли, у 4 больных аномалия вхождения ПА в канал на уровне С4, стеноз позвоночного канала — у одной больной. Возраст больных колебался от 28 до 74 лет.
Основными заболеваниями, на фоне которых развивались вестибулярные нарушения, были артериальная гипертония (АГ) в сочетании с атеросклерозом, вегетативно-сосудистая дистония, остеохондроз.
Всем больным проведено полное классическое отоневрологическое обследование, включающее исследование спонтанных и экспериментальных вестибулярных реакций (вращательная и калорическая пробы) и слуха. Исследование слухового анализатора проводилось с использованием аудиометрии и слуховых вызванных потенциалов.
Структурные изменения магистральных артерий головы (МАГ) и гемодинамические показатели кровотока по ПА и внутренней сонной артерии (ВСА) изучали с помощью ультразвукового дуплексного сканирования МАГ (ДС МАГ) с функциональными пробами, в ряде случаев при проведении спиральной компьютерной томографии (СКТ), магнитно-резонансой ангиографии.
Результаты
Отоневрологическое обследование позволило разделить больных на две группы: 45 больных с периферическим вестибулярным синдромом (ПВС) и 70 больных с центральным вестибулярным синдромом (ЦВС).
С целью выявления гемодинамических особенностей, на фоне которых развиваются ПВС и ЦВС, нами проводилось сопоставление наличия ПВС и ЦВС с состоянием кровотока по ПА по данным ДС МАГ (см. табл. на стр. 55 «Структурные изменения сосудов вертебрально-базилярной системы у больных с вертеброгенным головокружением»). Как видно из таблицы, ПВС сопровождался определенными структурными изменениями ПА — гипоплазия и асимметрия диаметров встречались наиболее часто.
ЦВС гетерогенны и развиваются у больных с вертебрально-базилярной недостаточностью на основе гипертонии, атеросклероза, диссекции ПА (спонтанной или травматической), приводящих к формированию мелких ишемических очагов в стволе головного мозга и мозжечке. Вестибулярные нарушения при центральном синдроме отличаются более тяжелым клиническим проявлением по сравнению с периферическим синдромом. При этом возможности компенсации нарушенных функций существенно снижены, вследствие непосредственного поражения вестибулярных ядер ствола. Установлено, что в патогенезе ЦВС важное значение имеет наличие у больных односторонних гемодинамически значимых стенозов и окклюзий ПА, двусторонних ее деформаций и извитостей (см. табл. на стр. 55 «Структурные изменения сосудов вертебрально-базилярной системы у больных с вертеброгенным головокружением»).
Механизм развития головокружения у пациентов с остеохондрозом шейного отдела позвоночника в 21 (45%) наблюдении обусловлен экстравазальной компрессией, которая была зарегистрирована на различных уровнях, чаще С3–С4, С5–С6 позвонков с обеих сторон. В 25 случаях (55%) была выявлена экстравазальная компрессия доминирующей ПА, причем у этой группы больных выявлялась симптоматика периферического кохлеовестибулярного синдрома на стороне компрессии. У этих же больных была выявлена гипоплазия одной ПА с другой стороны или асимметрия диаметров ПА с гемодинамическим преобладанием по одной из них.
Клинический пример
У больного 25 лет утром после сна появилось системное вращательное головокружение, тошнота, рвота, шум в левом ухе. Постепенно головокружение уменьшалось, но не исчезало несколько дней; любое изменение положения приводило к усилению головокружения, сохранялся шум в ухе.
При отоневрологическом осмотре в научно-консультативном отделении НЦ неврологии РАМН у больного выявлялась симптоматика со стороны левого мостомозжечкового угла: снижен роговичный рефлекс справа и чувствительность слизистой полости носа и полости рта (V пара черепно-мозговых нервов (ЧМН)), снижены вкусовые ощущения на передних 2/3 языка справа (VII пара ЧМН), односторонний спонтанный нистагм вправо. При проведении вращательной пробы отмечается асимметрия по лабиринту с раздражением справа и нейросенсорная тугоухость I степени.
Обоняние — не нарушено, в позе Ромберга — неустойчив, отклоняется влево, пальценосовую пробу выполняет с обеих сторон. При проведении ДС МАГ — диаметр левой ПА — 1,6 мм (гипоплазия), артерии проходимы, входят в канал на уровне С6 позвонка, имеют прямолинейный ход и стабильные показатели линейной скорости кровотока (ЛСК): справа 34 см/с, слева регистрируется низкоамплитудный кровоток в сегменте V3 — 7,4 см/с периферического типа (рис. 2).
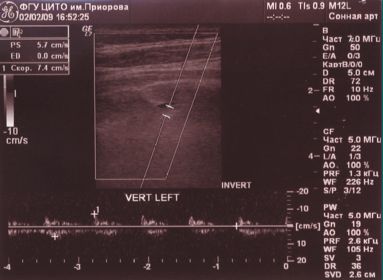
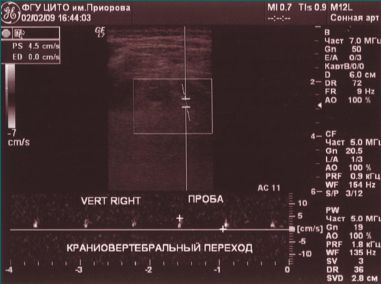
При проведении функциональных проб на уровне краниовертебрального перехода кровоток по правой ПА не регистрируется (рис. 3, 4).
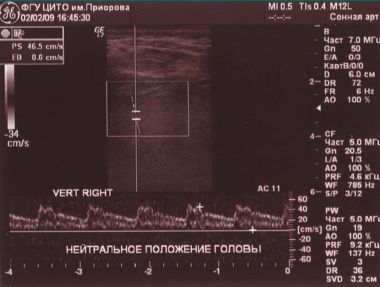
На рентгенограмме шейного отдела позвоночника выявлены изменения в виде смещения вперед позвонков С2–С4 по типу лестничных, определяется вариант Киммерли. Таким образом, головокружение и шум в ухе возникли у больного в результате недостаточности кровоснабжения в конечных артериях ВБС, обусловленной наличием структурных и гемодинамических изменений в ПА. Важным в этом клиническом случае является подтверждение снижения кровотока по ПА при дуплексном ультразвуковом исследовании, позволяющем выявить снижение кровотока при выполнении функциональных проб.
Периферическое головокружение (ПГ) может быть обусловлено болезнью Меньера, вирусным поражением вестибулярного ганглия и доброкачественным позиционным головокружением. В основе диагностики ПГ ишемической природы основное значение принадлежит результатам отоневрологического обследования, при котором выявляется не только симптоматика поражения внутреннего уха, но и других ЧМН, кровоснабжение которых осуществляется артериями ВБС.
Важное значение имеет сопоставление результатов отоневрологического обследования с результатами ДС ПА, которое проводится с применением функциональных проб, а также оценка состояния внутренних яремных вен на шее.
Дифференциальная диагностика
Своеобразие кохлеовестибулярных синдромов составляет основу дифференциальной диагностики заболеваний внутреннего уха и ретролабиринтной патологии (см. табл. на стр. 55 «Дифференциальная диагностика вестибулярных синдромов при болезни Меньера, центральном вестибулярном синдроме, периферическом вестибулярном синдроме и доброкачественном пароксизмальном позиционном головокружении»).
Лечение вертеброгенного вестибулярного головокружения
Терапия цервикального синдрома включает снятие болевого синдрома и мышечного напряжения. С этой целью рекомендованы нестероидные противовоспалительные препараты (НПВП), которые оказывают выраженное противовоспалительное и противоотечное действие. Массаж шейно-воротниковой зоны возможен только после уточнения структурных и гемодинамических изменений в магистральных сосудах головы.
Терапия вестибулярных нарушений включает вестибулолитические средства, которые назначаются до получения стойкого положительного эффекта, в среднем 2–3 месяца и более. Предпочтение отдается бетагистину гидрохлориду (Бетасерк), который обладает двойным механизмом действия: улучшает кровообращение внутреннего уха в ВБС, а также компенсаторные возможности вестибулярных ядер ствола головного мозга. Бетасерк обладает прямым стимулирующим действием на гистаминовые Н1-рецепторы внутреннего уха и опосредованное — на Н3-рецепторы вестибулярных ядер, нормализуя трансмиттерную передачу в нейронах медиальных ядер ствола головного мозга. Бетасерк нормализует нарушения вестибулярного аппарата, уменьшая выраженность головокружения, уменьшает шум в ушах, улучшает слух. Бетасерк назначают по 24 мг 2 раза в день после еды в течение нескольких месяцев. Препарат в дозе 48 мг в сутки эффективно уменьшает головокружение, практически не имеет противопоказаний, хорошо переносится пожилыми пациентами. Из побочных действий возможны легкие желудочно-кишечные расстройства, обычно быстро проходящие. Важное преимущество препарата — отсутствие седативного эффекта.
Выводы
-
Пациенты, страдающие остеохондрозом шейного отдела позвоночника и головокружением, лица молодого и трудоспособного возраста дополнительно могут иметь «мягкую» форму АГ, незначительные изменения ПА (односторонние гипоплазии, извитости, асимметрию диаметров), что приводит к развитию периферического головокружения.
-
Причиной возникновения приступа вестибулярного головокружения является раздражение лабиринта на фоне снижения кровотока по ПА и ее ветвям, в результате вынужденного длительного положение головы (повороты, наклоны вниз), а также затруднения венозного оттока из полости черепа.
-
Отоневрологический метод позволяет установить точный уровень поражения вестибулярного и слухового анализаторов с применением современных объективных методик вестибуло- и аудиометрии, исследование центральной гемодинамики и сопоставить полученные результаты с состоянием кровотока по ПА, установив ишемическую природу головокружения, что является залогом адекватной и успешной терапии головокружения.
-
Терапия вертеброгенного головокружения должна включать вестибулолитические средства, преимущественно — Бетасерк, который улучшает кровоснабжение внутреннего уха, ВБС и состояние вестибулярных структур ствола и мозжечка. Поскольку препарат обладает высокой эффективностью при вестибулярных нарушениях различной этиологии, включая вертеброгенную, и хорошо переносится в большинстве случаев, лечение Бетасерком может быть назначено как профильным специалистом — неврологом или ЛОР-врачом, так и терапевтом, еще до проведения занимающего достаточно много времени углубленного отоневрологического обследования, что позволит существенно повысить качество жизни пациента.
Литература
-
Верещагин Н. В. Патология вертебрально-базилярной системы и нарушения мозгового кровообращения. М.: Медицина. 1980.
-
Дадашева Н. Н. Неврологические аспекты вертеброгенного головокружения. М.: Аир-Арт. 2004. 32 с.
-
Алексеева Н. С. Вертебрально-базилярная недостаточность: центральные и периферические кохлеовестибулярные синдромы. Дисс. … доктора мед. наук; М., 2003.
-
Жукович А. В. Частная отоневрология. С-Пб. Медицина. 1966. с. 98–113.
-
Кусова Ф. У. Влияние повреждений и заболеваний шейного отдела позвоночника на состояние вертебробазилярной системы. Мат. симп. Повреждения и заболевания шейного отдела позвоночника. М. 2004, с. 19–21.
-
Bartels E., Flugel K. A. Evaluation of extracranial vertebral artery dissection with duplex color-flow imaging // Stroke. 1996. 27: 290–295.
-
Chung Y. S., Han D. H. Vertebro-basilar dissection: A possible role of whiplash injury in its pathogenesis // Neurol Res. 2002. 24: 129–138.
-
Czechowsky D., Hill M. D. Neurological outcome and quality of life after stroke due to vertebral artery dissection // Cerebrovasc Dis. 2002. 13: 192–197.
-
Dziewas R., Konrad C., Drager B., Evers S., Besselmann M., Ludemann P., Kuh-lenbaumer G., Stogbauer F., Ringelstein E. B. Cervical artery dissection-clinical features, risk factors, therapy and outcome in 126 patients // J Neurol. 2003. 250: 1179–1184.
-
Gray J. T., Puetz S. M., Jackson S. L., Green M. A. Traumatic subarachnoid haemorrhage: A 10-year case study and review // Forensic Sci Int. 1999. 105: 13–23.
-
Haldeman S., Kohlbeck F. J., McGregor M. Stroke, cerebral artery dissection, and cervical spine manipulation therapy // J Neurol. 2002. 249: 1098–1104.
-
Hanus S. H., Homer T. D., Harter D. H. Vertebral artery occlusion complicating yoga exercises // Arch Neurol. 1977. 34: 574–575.
-
Katirji M. B., Reinmuth O. M., Latchaw R. E. Stroke due to vertebral artery injury // Arch Neurol. 1985. 42: 242–248.
-
Konno K., Kurita H., Ito H., Shiokawa Y., Saito I. Extracranial vertebral artery dissection caused by scuba diving // J Neurol. 2001. 248: 816–817.
- Lewis M. J., Greenwood R. J., Brew S., Jager H. R. Economy class stroke syndromes; vertebral artery dissection revisited // J Neurol Neurosurg Psychiatry. 2003. 74: 1593–1597.
Н. С. Алексеева, доктор медицинских наук ГУ НЦ неврологии РАМН, Москва
