Соматическая патология у больных с неотложными состояниями, связанными с употреблением этанола
Продолжение. Начало см.: «Лечащий Врач», № 10, 2006 г.
Возможная соматическая патология у больных с неотложными состояниями, связанными с употреблением алкоголя, представлена поражением практически всех органов и систем организма.
Дыхательная система
Нарушения дыхательной системы при длительном алкогольном воздействии обусловлены повреждением отофарингеальной микрофлоры, нарушением механического и целлюлярного удаления микроорганизмов из легких, снижением гуморального и клеточного иммунитета. Практически всегда у больного с хронической алкогольной интоксикацией развивается хронический бронхит, а при достаточном стаже заболевания — пневмосклероз.
Характерной особенностью пневмоний у больных алкоголизмом является длительное ее течение без четкой клинической картины. Часто отсутствует лихорадка, воспалительные изменения лейкоцитарной формулы. У таких больных пневмонии имеют склонность к абсцедированию.
В случае острой алкогольной интоксикации (ОАИ) чаще всего имеет место аспирационная пневмония.
При алкогольном делирии также высока вероятность аспирационной пневмонии. Кроме того, очень вероятна нозокомиальная пневмония, развитию которой способствует длительная фиксация, седативная и антипсихотическая терапия, приводящая к выраженному нарушению дренажной функция трахеобронхеального дерева.
Особенности лечения пневмонии следующие:
- При симптоматической терапии пневмонии следует помнить, что применение парацетамола у злоупотребляющего алкоголем больного чревато развитием парацетамолового гепатита.
- Адреномиметические препараты в качестве бронхолитиков у такого больного имеют выраженный кардиотоксический эффект.
- Необходима антибактериальная терапия.
Внебольничные пневмонии чаще всего вызвают Streptococcus pneumoniae и Haemophilus influenzae, Klebsiella pneumoniae, различные энтеробактерии и легионеллы, Chlamydia pneumoniae, Staphylococcus aureus, Mycoplasma spp. Для них характерны постепенное развитие, медленное нарастание клинической картины. Как уже упоминалось, у больных алкоголизмом велика вероятность абсцедирования и эмпиемы плевры.
Препараты выбора:
- макролид + цефалоспорин III поколения;
- макролид + имипенем;
- макролид + ампициллин/сульбактам (или другие полусинтетические антибиотики,
- потенцированные ингибиторами β-лактамаз);
Антибиотики резерва представлены комбинацией: триметоприм/сульфаметоксазол + макролид.
В случае, когда возбудителем является золотистый стафилококк, назначают пенициллиназоустойчивые пенициллины или ванкомицин.
Аспирационную пневмонию чаще всего вызывают бактероиды, пептострептококки, фузобактерии, энтеробактерии, пневмококки.
Препараты выбора:
- клиндамицин или цефокситин;
- полусинтетический пенициллин/клавуланат.
Антибиотики резерва представлены комбинацией: клиндамицин + активные в отношении синегнойной палочки аминогликозиды.
Диагноз «госпитальная (нозокомиальная) пневмония» ставят в том случае, если пневмония выявлена не ранее чем через 48 ч после госпитализации, и доказано, что ее не было при поступлении.
Возбудителями госпитальной пневмонии чаще всего являются энтеробактерии (Enterobacter spp, Citrobacter spp.), актинобактерии, синегнойная палочка, легионелла, золотистый стафилококк.
Препараты выбора:
- пенициллин или цефалоспорин III поколения, активные в отношении синегнойной палочки, имипенем + аминогликозид, активный в отношении синегнойной палочки;
- фторхинолон + ампициллин/клавуланат;
- при выявлении метициллинрезистентных золотистых стафилококков — ванкомицин [6, 7].
Для злоупотребляющих алкоголем больных рекомендуются следующие препараты: фуразолидон, метронидазол, хлорпропамид, левомицетин, цефалоспорины, сульфаниламиды, обладающие тетурамоподобным действием.
Следует помнить, что изониазид и тетрациклины ускоряют поражение печени [8].
Сердечно-сосудистая система
Артериальная гипертензия является наиболее распространенной патологией сердечно-сосудистой системы у злоупотребляющих алкоголем больных.
Прием большого количества алкоголя или алкогольный абстинентный синдром (ААС) часто сопровождаются повышением артериального давления, что способно привести к поражению органов-мишений (гипертоническая энцефалопатия, острое нарушение мозгового кровообращения, острый коронарный синдром, острая сердечная недостаточность, расслаивающая аневризма аорты).
Особенности лечения:
- Гипертонический криз лечится по обычным схемам. При неосложненном течении терапия начинается с сублингвального приема нифидипина, при осложненном — с внутривенного введения эналаприлата.
- При развитии криза на фоне абстинентного синдрома целесообразно применение β-блокаторов (пропранолол).
- При наличии в крови этанола усугубляется гипотензивный эффект любых гипотензивных препаратов, b-блокаторы усиливают седативный эффект этанола, а нитроглицерин, клофелин и резерпин вызывают коллапсы с ослаблением коронарного кровотока [8].
ИБС. Несмотря на распространенное представление о том, что алкоголь «защищает» сосуды от атеросклероза, многочисленные исследования показали, что хроническая алкогольная интоксикация является независимым фактором риска развития ИБС (этанол стимулирует синтез триглицеридов и холестерина).
В низких дозах (12–15 г чистого этанола в сутки) этанол улучшает липидный профиль снижения агрегационной способности тромбоцитов. В наибольшей степени это благоприятное влияние выражено у мужчин 50–60 лет при употреблении в вышеприведенных умеренных дозах красного сухого вина.
Одновременно не подлежит сомнению тот факт, что продолжение приема алкоголя на фоне уже имеющейся ИБС ухудшает прогноз заболевания.
У таких больных алкоголь в сочетании с физической нагрузкой может приводить к безболевым инфарктам миокарда, во-первых, вследствие того, что алкоголь сам по себе является анестетиком, а во-вторых, из-за алкогольной невропатии, при которой первыми поражаются чувствительные нервные волокна [9].
Особенности лечения:
- Как уже упоминалось, нитроглицерин в сочетании с алкоголем вызывает ослабление коронарного кровотока.
- Наркотические анальгетики снижают летальную концентрацию этанола на 30–40%.
- У злоупотребляющих алкоголем больных усиливается эффект антикоагулянтов, кроме того, высок риск наличия язвенной болезни, что следует учитывать при решении вопроса о тромболизисе [8].
Алкогольная кардиомиопатия обычно развивается при злоупотреблении алкоголем в течение более 10 лет (в последнее время прослеживается четкая тенденция к снижению этого срока).
В патогенезе поражения сердца участвуют два механизма: инфильтрация миокарда жировой тканью с дегенерацией кардиомиоцитов и тиаминзависимое поражение вегетативной нервной системы.
Алкогольный эксцесс сам по себе является провоцирующим фактором развития как изолированной мерцательной аритмии (синдром «праздничного сердца»), так и развернутой клинической картины алкогольной кардиомиопатии (нарушение ритма, недостаточность кровообращения по большому и малому кругу).
Морфологическая картина алкогольной кардиомиопатии складывается из группы патологических проявлений, в число которых входят:
- гипертрофия миокарда,
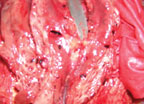
- липоматоз миокарда (рис. 1),
- мелкоочаговый кардиосклероз,
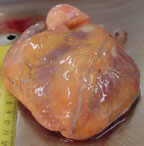
- расширение полостей сердца (рис. 2),
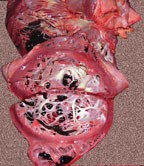
- гиперэластоз эндокарда (рис. 3),
- образование внутрисердечных тромбов,
- застойная сердечная недостаточность.
Особенности лечения:
- Основные принципы терапии такие же, как и при лечении дилатационной кардиомиопатии другой этиологии. Необходимым условием эффективности лечения является отказ от употребления алкоголя.
- Особенно важно введение больших доз тиамина.
- В качестве урежающих ритм препаратов при мерцательной аритмии предпочтительны β-блокаторы. Сердечные гликозиды у таких больных обладают выраженным проаритмогенным действием.
- Петлевые диуретики способны усилить уже имеющуюся гипокалиемию и провоцировать нарушения ритма [8].
Желудочно-кишечный тракт
|
| Рисунок 1. Стромальный липоматоз миокарда |
|
| Рисунок 2. Дилатированные камеры сердца |
|
| Рисунок 3. Гиперэластоз эндокарда левого желудочка. Истончение стенок и дилатация сердца |
Поражение слизистой желудка в виде алкогольного гастрита или язвы обусловлено прямым токсическим воздействием не только алкоголя, но и ацетальдегида, образующегося при участии алкогольдегидрогеназы IV типа. Этот фермент находится в слизистой желудка и метаболизирует 19% поступающего этанола, окисляя его до ацетальдегида [9].
Таким образом, злоупотребление алкоголем является независимым фактором риска развития язвенной болезни желудка и двенадцатиперстной кишки, осложняет течение Helicobacter pylory-ассоциированного поражения слизистой, препятствует рубцеванию язвы, способствует ее рецидивированию.
В связи с уже упоминавшейся алкоголь-ассоциированной полиневропатией, а также склонностью к «обезболиванию» алкоголем у таких больных повышен болевой порог, и обострение заболевания может проявляться язвенным кровотечением.
Другие более редкие причины желудочно-кишечного кровотечения у больных с хронической алкогольной интоксикацией — синдром Меллори–Вейса (надрыв слизистой кардиального отдела пищевода в результате упорной рвоты), синдром Берхава (разрыв всех слоев пищевода) и кровотечение из варикозно-расширенных вен пищевода. Синдром Меллори–Вейса и синдром Берхава нередко развиваются на фоне ААС, для которого характерна повторная рвота. Если у больного с клиникой ААС вместо гипертонии регистрируется гипотония, в первую очередь необходимо исключить желудочно-кишечное кровотечение.
Особенности лечения:
- Антисекреторные препараты снижают активность алкогольдегидрогеназы желудка и усиливают всасывание алкоголя.
- Назначение антисекреторных препаратов необходимо при алкогольном делирии независимо от наличия верифицированной язвенной болезни и поражения печени.
Печень. Гепатоцит — основное место, где происходит окисление этанола с образованием ацетальдегида, поэтому основной удар приходится именно на печень. Наибольшие изменения наблюдаются в центролобулярной зоне, в этой же зоне происходит некроз гепатоцитов.
Жировая дистрофия печени — потенциально обратимое состояние, развивается при употреблении 50–60 г чистого этанола ежедневно.
|
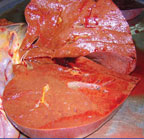
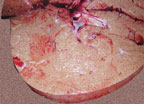
| Рисунок 4. Алкогольный жировой гепатоз |
|
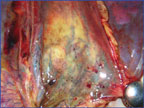
| Рисунок 5. Алкогольный гепатит |
|
| Рисунок 6. Варикозные вены пищевода |
| Рисунок 7. Цирроз печени. Спленомегалия |
Морфологически отмечается накопление жира в гепатоцитах вследствие остановки окисления жирных кислот, вызываемой алкоголем (рис. 4). Наряду с крупнокапельным ожирением гепатоцитов, имеют место перицеллюлярный фиброз вокруг центральных вен, нейтрофильная инфильтрация междольковых, а иногда и внутридольковых (вокруг гепатоцитов) отделов печени, набухание гепатоцитов, отложение в них гиалиновых телец Мэллори [9].
Клиническое течение самого жирового гепатоза обычно бессимптомное. Отмечается увеличение содержания в сыворотке крови g-глутамилтранспептидазы, умеренное повышение активности сывороточных трансаминаз и щелочной фосфатазы. Прекращения приема алкоголя обычно достаточно для полной регрессии заболевания.
Острый алкогольный гепатит (рис. 5) обычно развивается в случае, когда печень не способна метаболизировать индивидуально токсическую дозу этанола. Чаще всего развивается вместе с ААС. Возможно фульминантное (молниеносное) течение заболевания с крайне неблагоприятным прогнозом. При фульминантном гепатите быстро развивается печеночная энцефалопатия, вероятно развитие портальной гипертензии по синусоидальному типу, геморрагического и гепаторенального синдромов.
Лечение острого алкогольного гепатита проводится параллельно с терапией ААС, так как отказ от алкоголя является непременным условием эффективности лечения.
- Проводится инфузия 10% глюкозы с добавлением адеметионина — гептрала, который относится к группе гепатопротекторов с антидепрессивной активностью, обладает детоксикационным, регенерирующим, антиоксидантным, антифиброзирующим и нейропротекторным действием [8].
- Внутривенно вводятся витамины группы В и аскорбиновая кислота.
- Восполняется дефицит калия и магния.
- При тяжелом течении заболевания и в отсутствие желудочно-кишечного кровотечения возможно применение преднизолона в дозе до 300 мг в сутки.
Алкогольный цирроз печени развивается при потреблении 80–100 г этанола в сутки в течение 10–15 лет.
У больных с хронической алкогольной интоксикацией цирроз печени может формироваться на фоне фиброза без промежуточного этапа в виде алкогольного гепатита.
Фиброз развивается в результате трансформации жировых клеток Ито (липоцитов печени) в фибробласты и миофибробласты. Синтез коллагена стимулируется гипоксией и некрозом клеток, а также продуктами перекисного окисления липидов [9].
Так как цирроз печени — необратимое состояние, терапия должна быть направлена на предупреждение и коррекцию осложнений, от которых больные и погибают. Осложнения включают ряд синдромов.
Синдром портальной гипертензии, проявляющийся варикозным расширением вен пищевода (рис. 6), желудка, геморроидального сплетения, кровотечениями из расширенных вен, спленомегалией (рис. 7, 8). Характерно развитие венозных коллатералей передней брюшной стенки.
Лечение предполагает применение:
- β-блокаторов (анаприлин);
- пролонгированных нитратов (несовместимы с алкоголем);
- антацидов;
- склеротерапии; шунтирующих операций.
Желтуха свидетельствует о превалировании процесса разрушения гепатоцитов над процессами регенерации и потому является плохим прогностическим признаком.
Отечно-асцитический синдром проявляется скоплением жидкости в брюшной полости и периферическими отеками.
Лечение включает:
- бессолевую диету;
- мочегонные препараты (препарат выбора — верошпирон);
- лечебный лапароцентез (при эвакуации большого количества жидкости увеличивается риск развития энцефалопатии).
Синдром печеночной энцефалопатии проявляется нарушением циклов сна и бодрствования, конструктивной апраксией, хлопающим тремором. При прогрессировании нарастают нарушения сознания вплоть до печеночной комы.
Назначаются:
- безбелковая диета;
- лактулоза;
- деконтаминация кишечника;
- орнитин (гепа-мерц).
Синдром нарушения белково-синтетической функции печени проявляется гипоальбуминемией, гипопротеинемией, кровоточивостью (рис. 9).
Лечение включает:
- инфузию альбумина, свежезамороженной плазмы;
- викасол.
Гепаториенальный синдром проявляется прогрессирующей почечной недостаточностью.
Лечение предполагает экстракорпоральную детоксикацию.
Поджелудочная железа. В настоящее время принято считать дебют алкогольного панкреатита потенциально обратимым острым панкреатитом, который, однако, при продолжении алкоголизации ведет к необратимому изменению поджелудочной железы.
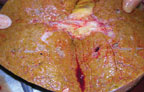
|
| Рисунок 8. Мелкоузловой цирроз печени |
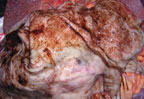
|
| Рисунок 9. Кровотечение из острых эрозий желудка |
|
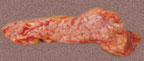
| Рисунок 10. Индуративный панкреатит с очагами стеатонекроза |
Алкоголь и его метаболиты (ацетальдегид) влияют на сфинктер Одди, протоки железы, ацинарные клетки железы, вызывая внутрипротоковую гипертензию. Обычно злоупотребление алкоголем в течение нескольких лет приводит к осаждению белков внутри протоков поджелудочной железы. Со временем отложения белков становятся более распространенными, что вызывает гистологические изменения. Через 3–5 лет развивается первый клинический приступ панкреатита, обусловленный преждевременной активацией ферментов поджелудочной железы. При этом трипсин и фосфолипаза А2 обусловливают некроз тканей, эластаза — разрушение стенок кровеносных сосудов и геморрагический синдром [9].
Алкогольный панкреатит возникает при длительном ежедневном приеме не менее 100–120 мг чистого этанола, однако возможен и после однократного массивного «возлияния» без алкогольного анамнеза (рис. 10). Различают отечную и некротическую формы панкреатита. При отечном панкреатите воспаление ограничивается поджелудочной железой, летальность составляет 5%. При некротическом панкреатите воспалительный процесс выходит за пределы железы, повышая летальность до 50%. В первые несколько дней смерть наступает вследствие шока, почечной недостаточности, респираторного дистресс-синдрома легких (фосфолипаза А2 повреждает альвеолярные мембраны легких).
После первой недели заболевания прежде всего опасны осложнения некроза поджелудочной железы: вторичное инфицирование нежизнеспособных тканей (обычно, грамотрицательная флора), кистоид поджелудочной железы — скопление панкреатической жидкости и тканевого детрита, отграниченное капсулой из фиброзной стенки и сосудов, опасный инфицированием, кровотечением и перфорацией.
Характер течения алкогольного панкреатита непостоянен, в первые годы часто отмечается его рецидивирующее течение, а по мере прогрессирования панкреатита, гибели паренхимы поджелудочной железы заболевание приобретает безрецидивное течение с постоянными болями и функциональными расстройствами: внешнесекреторной панкреатической недостаточностью; скрытым или явным сахарным диабетом, реже — гипогликемическим синдромом; симптомами холестаза; нарушениями дуоденальной проходимости; сегментарной портальной гипертензией; воспалительными и гнойными осложнениями.
Лечение острого алкогольного панкреатита и обострения хронического панкреатита часто приходится проводить одновременно с лечением ААС (часто осложненного алкогольным делирием, что значительно утяжеляет состояние больного и ухудшает прогноз). В таких случаях к терапии по возможности присоединяют транквилизаторы, антипсихотические препараты, β-адреноблокаторы, восполняют дефицит витаминов, прежде всего группы В.
Консервативное лечение обычно позволяет купировать атаку отечного (интерстициального) острого панкреатита и предотвратить развитие «хирургических» осложнений при ограниченном неинфицированном панкреонекрозе.
Базовая терапия предусматривает:
- прекращение приема пищи и жидкости через рот, декомпрессию желудка; местное применение холода;
- инфузии солевых растворов и 5% глюкозы;
- применение антибиотиков широкого спектра действия;
- назначение анальгетиков (наиболее эффективно купировать болевой синдром и парез кишечника с помощью эпидуральной анестезии);
- ингибирование панкреатических ферментов (антипротеазы, свежезамороженная плазма);
- применение антисекреторных препаратов.
Комплекс интенсивной терапии при панкреонекрозе с органной недостаточностью включает современные методы детоксикации, продленной искусственной вентиляции легких, возмещение дефицита жидкости, электролитов, белкового состава крови, устранение анемии, парентеральное и энтеральное зондовое питание, инсулинотерапию.
Показаниями к операции при остром панкреатите являются:
- клиническая картина «острого живота» — если нет возможности исключить другое острое хирургическое заболевание;
- деструктивный холецистит;
- обтурационная желтуха, холангит;
- прогрессирование полиорганной недостаточности, несмотря на интенсивную терапию;
- инфицирование некротизированных участков поджелудочной железы и парапанкреатической клетчатки;
- осложнения панкреонекроза: кровотечения, желудочные и кишечные свищи, перитонит, кишечная непроходимость, псевдокисты.
Возможности консервативного лечения в хронической фазе панкреатита ограничены. Поэтому основные усилия должны быть направлены на смягчение болей, рациональную диетотерапию, коррекцию внешне- и внутрисекреторной недостаточности поджелудочной железы (ферментные и сахароснижающие препараты), а также на устранение этиологических факторов панкреатита — воздержание от приема алкоголя.
Миоренальный синдром у злоупотребляющих алкоголем больных — вариант crush-синдрома — вызывается позиционной травмой. Причиной такой травмы является длительное пребывание в одной и той же позе, часто противоестественной, что возможно в состоянии алкогольной интоксикации, когда алкоголь играет роль анестетика. Важным фактором является наличие периферической полинейропатии, при которой первыми поражаются чувствительные нервные волокна. В таких случаях миоренальный синдром манифестирует вместе с ААС, при котором основные жалобы — изменение мочи, боль и отек конечности — «маскируются» массой жалоб, связанных с абстиненцией.
Проявлениями миоренального синдрома являются рабдомиолиз и острая почечная недостаточность.
Клинически характерны быстро нарастающий деревянистый отек поврежденной конечности, нарушение чувствительности, появление грязно-бурой мочи.
В олигоанурической стадии (до 3 нед) на первый план выступают симптомы уремии. Часто на этой стадии развивается алкогольный делирий. При благоприятном исходе наступает фаза ранней полиурии и восстановления функции почек.
Лечение осуществляется в отделении интенсивной терапии, где имеется возможность проведения экстракорпоральной детоксикации [9].
Таким образом, у больного, перенесшего алкогольный эксцесс, часто встречаются как проявления ОАИ или ААС различной степени тяжести, так и различная соматическая патология в стадии декомпенсации, взаимно усиливающие друг друга. Отсутствие единых стандартов ведения таких больных и «пограничность» проблемы определяют сложность выбора лечебной тактики, что, в свою очередь, повышает смертность, пролонгирует время пребывания больного в стационаре и увеличивает риск осложнений.
Литература
- Шестоперова Ю. 9 литров на крышку гроба// Московский комсомолец, 19.05.2006.
- Нейрохимия/ под ред. И.П. Ашмармна/ М.: Издательство Ин-та биомедицинской химии РАМН, 1996. С. 415–423.
- Лужников Е. А., Костомарова Л. Г. Острые отравления: руководство для врачей. М.: Медицина, 1989. С. 278–286
- Кекелидзе З. И., Земсков А. П., Филимонов Б. А. Тяжелый алкогольный делирий//РМЖ. Т. 6. № 2. 1998. http://www.rmj.ru/rmj/t6/n2/4.htm.
- Кекелидзе З. И., Чехонин В. П. Критические состояния в психиатрии. М, 1997. С. 119–156.
- Никонова Е. В., Чучалин А. Г., Черняев А. Л. Пневмонии: эпидемиология, классификация, клинико-диагностические аспекты// РМЖ. 1997. Т. 5. № 17. С.1095–1099.
- Сэнфорд Дж., Гилберт Д., Гербердин Дж. и др. Антимикробная терапия: пер. с англ. М.: Практика, 1996. С. 31–2.
- Видаль. 2006 http://www.vidal.ru/vidal_2006/ info/drugs/d_3275.htm.
- Огурцов П. П., Жиров И. В. Неотложная алкогольная патология. СПб.: Невский Диалект, 2002. 118 с.
- Громова О. А. Нейрометаболическая фармакотерапия. М., 2000. 53 с.
В. Г. Москвичев, кандидат медицинских наук
Р. Ю. Волохова
А. Л. Верткин, доктор медицинских наук, профессор
МГМСУ, ННПОСМП, Москва

