Применение препарата атеростат (симвастатин) у больных с гиперлипидемией
Терапия статинами признана кардиологами всего мира в качестве необходимой составляющей лечения при артериальной гипертонии и ишемической болезни сердца (ИБС). Она проводится в качестве профилактики тяжелых осложнений заболевания [1, 3]. При неизменной востребованности этих препаратов основным фактором, препятствующим широкому применению терапии статинами, является их высокая рыночная стоимость. Появление в настоящее время дженерических препаратов симвастатина дает возможность сделать необходимую терапию доступной для большинства нуждающихся в ней пациентов. Однако широкое использование дженериков в клинике требует достоверного подтверждения их клинической эффективности и безопасности.
Целью настоящего исследования была оценка эффективности и безопасности препарата атеростат (симвастатин) (Сти-Мед-Сорб) у больных с гиперлипидемией фенотипов Ia, IIb, III, не получавших до этого препаратов группы статинов и других гиполипидемических средств.
В исследование были включены 40 больных (27 мужчин, 13 женщин) в возрасте от 38 до 81 года (средний возраст 64 ± 9 лет) с диагнозом «гиперлипидемия», которые прежде никогда не принимали гиполипидемическую терапию. Все участвующие в исследовании больные проходили общий клинический осмотр (с обязательным измерением веса, расчетом индекса массы тела (ИМТ), объема талии, артериального давления, частоты сердечных сокращений). Проводились оценка таких факторов риска развития сердечно-сосудистых заболеваний (ССЗ), как возраст, курение, артериальная гипертензия, избыточный вес, сахарный диабет, а также распределение по категориям риска развития фатальных осложнений, предложенным Европейскими рекомендациями по профилактике ССЗ. В сыворотке крови определяли общий холестерин, триглицериды, холестерин липопротеинов высокой плотности (ЛПВП) и липопротеинов низкой плотности (ЛПНП). Последний показатель рассчитывали по формуле Фридвальда при концентрации триглицеридов, не превышающей 4,5 ммоль/л:
ЛПНП = оХС — (ЛПВП + (ТГ/2,2))(ммоль/л),
где оХС — общий холестерин, ТГ — триглицериды.
Коэффициент атерогенности (КА) рассчитывался по формуле: (оХС — ЛПВП)/ЛПВП (по А. Н. Климову). Помимо липидного профиля, оценивалась безопасность терапии атеростатом путем контроля активности печеночных ферментов: аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), g-глютамата (ГГТ), щелочной фосфатазы (ЩФ), лактатдегидрогеназы (ЛДГ), билирубина, а также контроля креатинфосфокиназы (КФК), креатинина, мочевины и концентрации глюкозы.
После клинического обследования и определения липидного профиля у всех привлеченных больных определялась категория риска, согласно рекомендациям по профилактике ССЗ Европейского общества кардиологов. Первой категории (высокий риск) соответствовали 22 (55 %) больных с клиническими проявлениями ИБС. Ко 2-й категории (умеренный риск) принадлежало 5 (12,5 %) больных без клинических проявлений ССЗ, однако с несколькими факторами риска ( ≥ 2). Третью категорию (низкий риск) составили 13 (32,5 %) больных без клинических проявлений ССЗ с одним умеренно выраженным фактором риска.
Согласно Фрамингемской шкале оценки сердечно-сосудистого риска, общий бал риска привлеченных пациентов составил 14,25 ± 7,6.
При отсутствии противопоказаний (отсутствие повышения АСТ и АЛТ в 2 и более раз, активности КФК в 5 и более раз, нарушения функции почек) больным назначался атеростат в дозе 20 мг однократно в вечернее время после ужина. Переносимость препарата оценивали с учетом жалоб больного и данных физикального осмотра.
Контрольную группу составили 16 больных (6 мужчин и 10 женщин) в возрасте от 56 до 82 лет (средний возраст 65,4 ± 6,7 лет), не получавших атеростат.
Больные обеих групп достоверно не отличались по таким показателям, как возраст, вес, ИМТ, уровень артериального давления, анамнез и липидный профиль. У 1 больного в анамнезе был сахарный диабет 2 типа средней тяжести. Частота абдоминального ожирения, устанавливавшаяся на основании измерения объема талии: более 88 см — отмечена у 12 (92,3 %) женщин, более 102 см — у 8 (29,6 %) мужчин. Средний вес больных составил 81,8 ± ±15 кг, а ИМТ — 28,3 ± 4,1 кг/м2. Нормальный ИМТ был выявлен лишь у 11 (27,5 %) из 40 больных.
Период наблюдения больных составил 12 нед. Через первые 6 нед после начала терапии оценивались липидный профиль и биохимические параметры. При достижении целевых уровней холестерина ЛПНП и при отсутствии негативных изменений биохимических параметров, а также при хорошей переносимости препарата лечение продолжали в прежних дозах.
Все пациенты соблюдали гипохолестеринемическую диету.
Сравнение средних значений параметров в исследуемых группах, а также динамика их изменений по результатам исследований оценивались по парному Т-критерию Стьюдента.
Через 6 нед после начала приема атеростата в дозе 20 мг в сутки наблюдалось достоверное изменение уровня общего холестерина, ЛПНП, ЛПВП, триглицеридов и КА.
Через 12 нед от начала терапии препаратом не было выявлено достоверного изменения уровня артериального давления и частоты сердечных сокращений (ЧСС), но наблюдалось достоверное снижение общего холестерина (на 26 %), триглицеридов (на 34%), холестерина ЛПНП (на 33 %) и КА (на 26 %) (табл. 1). Наблюдалось также достоверное снижение риска сердечно-сосудистых осложнений по Фрамингемской шкале с14,25 ± 7,6 исходно, до 10,9 ± 6,3 баллов (p < 0,001).
|
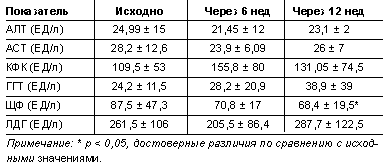
| Таблица 2. Динамика показателей сывороточных ферментов в процессе лечения атеростатом |
Не отмечалось изменений со стороны печеночных ферментов, а именно АСТ, АЛТ, КФК, ЩФ и ГГТ (табл. 2). У двух больных наблюдалось повышение ГГТ в 3 раза к 12-й неделе лечения атеростатом. У 1 больного через 6 нед от начала лечения было отмечено увеличение КФК в 2 раза по сравнению с исходными данными, что, однако, не потребовало отмены препарата. Хотя изменения ЩФ были достоверными, эти значения укладываются в ранг нормальных величин (от 3 до 120 ЕД/л).

|
| Таблица 3. Динамика показателей креатинина и мочевины при лечении атеростатом среди больных основной и контрольной групп |
Отсутствие достоверных изменений со стороны креатинина свидетельствует о неизменности функции почек (табл. 3).
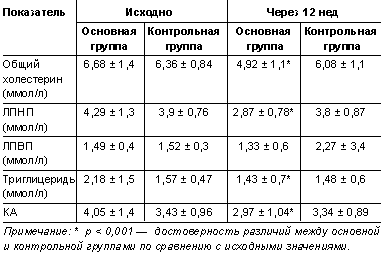
Мы сравнили динамику биохимических показателей в процессе лечения атеростатом с данными больных контрольной группы. Через 12 нед от начала лечения в обеих группах не наблюдалось достоверных изменений со стороны артериального давления и ЧСС. Что касается липидного профиля, то через 12 нед лечения и наблюдения между двумя группами имелось достоверное отличие по уровню общего холестерина (на 19 %), триглицеридов (на 3 %), холестерина ЛПНП (на 24 %) и КА (на 11%) (табл. 4).
|
| Таблица 4. Динамика показателей липидного профиля среди больных основной и контрольной групп в процессе наблюдения и лечения атеростатом |
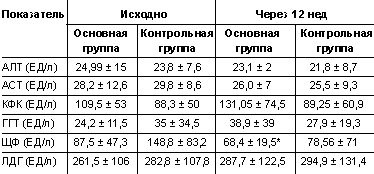
На 12-й неделе наблюдения показатели печеночных ферментов у обеих групп достоверных изменений не претерпели, что свидетельствкет о безпасности препарата при назначении его в средней дозе 23 мг/сут (табл. 5).
Как видно из таблицы 5, в основной группе показатели печеночных ферментов при применении атеростата достоверно не отличались от данных, полученных у больных, которые не принимали атеростат, что свидетельствует о безопасности препарата при назначении его в средней дозе 23 мг в сутки.
|
| Таблица 5. Динамика показателей сывороточных ферментов исходно и через 12 нед в основной и контрольной группах |
Атеростат хорошо переносился больными и не вызывал клинически значимых нежелательных явлений. При опросе больных мы выявили единичные побочные эффекты в виде изжоги, тошноты, боли в животе, сонливости, судорог в ногах, головокружения, двое больных отметили запор. Эти побочные эффекты сопоставимы с наиболее часто встречающимися при применении статинов [2].
Таким образом, можно отметить, что атеростат обладает требуемой эффективностью, безопасностью и хорошей переносимостью как у лиц с клинически выраженной ИБС, так и без клинических проявлений ИБС. При применении атеростата наблюдается достоверное снижение липидов крови, не повышается уровень печеночных ферментов и достаточно редко встречаются побочные явления.
С появлением в России доступных препаратов из группы статинов становится более возможным выполнение задач не только по лечению повторных сердечно-сосудистых осложнений, но и по их успешной профилактике у больных без клинически выраженной ИБС и с высоким суммарным риском сердечно-сосудистых осложнений [3, 4]. Настоящее исследование подтвердило, что атеростат обладает требуемой эффективностью, безопасностью и хорошей переносимостью как у лиц с клинически выраженной ИБС, так и без клинических проявлений ИБС.
Литература
- Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации. Разработаны комитетом экспертов ВНОК. М., 2004.
- Гендлин Г. Е. Статины в лечении сердечно-сосудистых заболеваний//Сердце. 2005. Т. 4. № 3 (21). С.170.
- Welch K. M. A. Statins for the prevention of cerebrovascular disease: the rational for robust intervention// Eur Heart J. 2004; 6С :34–42.
- Brown W. V. Managing dyslipidemia — multiple patients and multiple approaches: metabolic syndrome, familial hypercholesterolaemia and hypertension// Eur Heart J. 2004; 6A : 23–27.
В. Н. Ларина, кандидат медицинских наук
Б. Я. Барт, доктор медицинских наук, профессор
РГМУ, Москва
Врезки:
